Global Point of Care
Oberoende studie bekräftar
att Afinion™ 2 levererar
patientnära HbA1c-resultat
av laboratoriekvalitet
Patientnära HbA1c-analys av laboratoriekvalitet
Mätnoggrannhet vid HbA1c-analys är avgörande vid diagnostisering och behandling av diabetes. Även om många patientnära analysinstrument (PNA (patientnära analys)) är certifierade av International Federation of Clinical Chemistry (IFCC) och National Glycohemoglobin Standardization program (NGSP), innebär certifieringen inte nödvändigtvis att de presterar lika bra i verkliga kliniska situationer.
En nyligen genomförd oberoende studie utvärderade 19 PNA HbA1c-instrument, vilka visade betydande variationer i analytisk kvalitet. Analysinstrumentet Afinion™ 2 utmärker sig som en toppresterande analysmetod med resultat som uppfyllder eller till och med överträffar samtliga viktiga prestandakriterier.
Sammanfattning av oberoende studie: Jämförelse av 19 PNA HbA1c-instrument
Denna studie, utförd av Lenters-Westra med flera, utvärderade prestandan hos 19 patientnära HbA1c-instrument, inklusive en jämförelse mot certifieringskriterierna från International Federation of Clinical Chemistry and Laboratory Medicine- (IFCC) och National Glycohemoglobin Standardization Program (NGSP).1 IFCC- och NGSP-organisationerna certifierar HbA1c-analyser för att säkerställa mätnoggranheten och de standardiserade analysresultat för en tillförlitlig diagnos och behandling av diabetes. De patientnära analysinstrumenten jämfördes med fyra laboratoriebaserade referensmetoder som används för tillverkarcertifiering vid det europeiska referenslaboratoriet för glykosylerat hemoglobin (ERL).
Författarna av studien har tidigare genomfört flera prestandautvärderingar på
PNA-instrument med fastställda kvalitetskriterier, och analysinstrumentet Afinion har konsekvent presterat bra.2,3
Studien utfördes i två faser, där varje fas utvärderade 10 instrument. Afinion 2 ingick i båda faserna och fungerade som ett referensinstrument för att säkerställa jämförbarheten i studien. HbA1c-koncentrationer testades över hela det diagnostiska området, inklusive normala nivåer, prediabetes och diabetes.
Viktiga resultat: Afinion 2 visade högst mätnoggranhet vid HbA1c-analyserna
- Afinion 2 uppnådde CVs ≤2,0 % i NGSP-enheten och CVs ≤3,0 % i IFCC-enheten. Analysinstrumentet Afinion 2 uppnådde CVs ≤2,0 % i NGSP-enheten och CVs ≤3,0 % i IFCC-enheten på alla testade koncentrationsnivåer. Endast två andra instrument uppfyllde dessa kriterier i NGSP-enheten, och endast en annan instrument uppfyllde kriterierna i IFCC-enheten.
- Afinion 2 uppfyller IFCC- och NGSP-certifieringskriterier. Årlig certifiering är eventuellt inte en tillräcklig indikation på kvalitet eftersom många av PNA instrumenten var IFCC- och/eller NGSP-certifierade, men det var endast fem instrument som uppfyllde båda prestandakriterierna när de testades i denna studie.

- Afinion 2 var det enda instrument som uppfyllde alla IFCC-kriterier, vilket indikerar att den även är lämplig för kliniska studier. Tio PNA instrument uppfyllde minimum IFCC-standarden för rutinmässig klinisk användning (>2σ), medan Afinion 2 var det enda instrument som uppfyllde även de strängare IFCC-kriterierna, vilket visar att det är lämpligt för användning även för kliniska studier (>4σ).
- Analytical performance has important implications for clinical care. Some of the devices showed significant negative bias that could lead to misdiagnosis or incorrect management decisions
Detaljerade resultat: Analytiska prestandamått för HbA1c-instrument
Precision
- Afinion 2, Atellica DCA och On Call MultiPro var de enda tre av de
19 PNA-instrumenten som utvärderades som uppfyllde CVs ≤2,0 % beräknade i NGSP-enheten vid samtliga testade HbA1c-koncentrationsnivåerna (30, 48 och 75 mmol/mol). - Endast Afinion 2 och Atellica DCA uppfyllde CVs ≤3 % beräknade i IFCC/
SI-enheten vid alla tre testade koncentrationsnivåer (30, 48 och 75 mmol/mol).
Riktighet (bias)
- Bias beräknades vid tre koncentrationsnivåer: 30, 48 och 75 mmol/mol HbA1c (5,0 %, 6,5 % och 9,0 %).
- Afinion 2 visade en liten avvikelse gentemot medelvärdet hos de fyra referens metoderna från -1,3 till -0,7 mmol/mol (-0,12 till -0,06 % HbA1c).
IFCC-kriterier
- IFCC-certifieringskriterier kräver att det beräknade sigma-värdet blir >2σ för rutinmetoder och >4σ för användning vid kliniska studier. Sigma beräknas med hjälp av bias, CV och ett totalt tillåtet fel (TAE) inställt på 6,9 % (10 % i SI-enheter) med formeln: Sigma = (TAE - bias)/CV.
- Afinion 2 var det enda PNA-instrumentet som uppfyllde det strängare
>4σ-kriteriet. Det fanns 10 instrument som uppfyllde kriterierna för rutinmässig klinisk användning (>2σ).
NGSP-kriterier
- NGSP-certifieringskriterier kräver att 36 av 40 resultat ligger inom ±5 % jämfört med de laboratoriebaserade referensmetoderna.
- Afinion 2 och QuoLab var de enda två PNA-instrument som uppfyllde
NGSP-kriterierna med de fyra laboratoriebaserade referensmetoderna i fas 1. I fas 2 uppfyllde Afinion 2 kriterierna med alla utom en referensmetod (Tosoh G11). - Endast fem (Afinion 2, cobas b 101, QuoLab, Atellica DCA, On Call MultiPro) av de 19 PNA-instrumenten uppfyllde NGSP-kriterierna med minst en av de laboratoriebaserade referensmetoderna.
HbA1c-prover med hög koncentration
- Studien testade HbA1c-prover från 103 mmol/mol (11,6 %) till 148 mmol/mol (15,7 %). Detta är en användbar utvärdering eftersom externa program för kvalitetsbedömning (EQA) som till exempel sådana som administreras av College of American Pathologists (CAP) inte regelbundet utvärderar prover med höga HbA1c-koncentrationer.4
- Afinion 2 uppvisade små skillnader i prover med höga HbA1c-koncentrationer jämfört med den laboratoriebaserade referensmetoden, Tosoh G8, i intervallet -2,1 % till 2,3 % skillnad.
Hemoglobinvarianter
- Eftersom studien använde frysta prover, som inte kan analyseras med Afinion 2, kunde instrumentet inte utvärderas för interferens på hemoglobinvarianter.
- Det bör dock noteras att Afinion 2 tidigare inte har uppvisat någon signifikant interferens från hemoglobinvarianter, med undantag för höga koncentrationer (>10 %) av HbF. Analysprincipen för Afinion 2 (boronataffinitet) är okänslig för hemoglobinvarianter.5
Sammanfattning av viktiga prestandakriterier
I tabellen nedan sammanfattas prestandan för alla 19 PNA-instrument gentemot de kriterier som fastställts i studien.
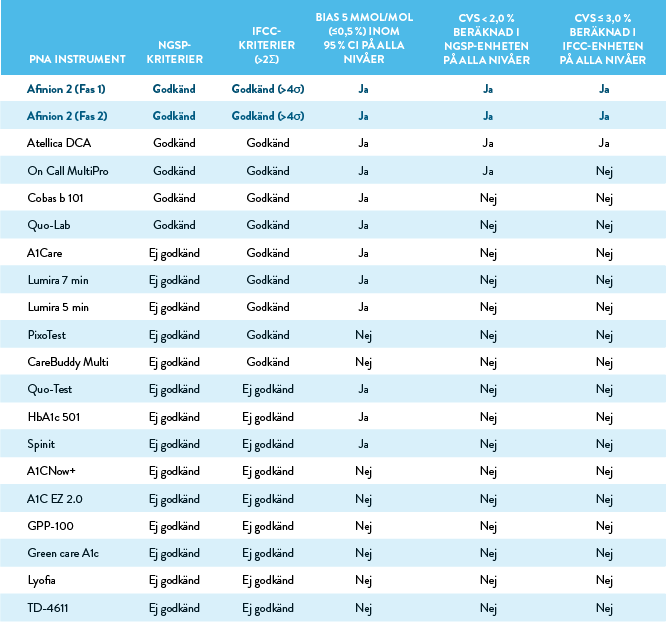


NGSP-certifieringskriterierna kräver att minst 36 av 40 prover ligger inom ±5 % av resultaten från minst en laboratoriebaserad referensmetod. För IFCC-kriterierna gäller >2σ för rutinmetoder och >4σ för användning vid kliniska studier, enligt formeln: Sigma = (TAE - bias)/CV, där TAE (totalt tillåtet fel) är angett som 6,9 % (10 % i SI-enheter), bias mäts vid 6,5 % HbA1c (48 mmol/mol) enligt CLSI EP-9-A3 och CV mäts vid 6,5 % HbA1c (48 mmol/mol) enligt CLSI EP-15-A3. Bias utvärderades vid 3 HbA1c koncentrationer 30, 48, och 75 mmol/mol (5,0 %, 6,5 % och 9,0 %). Författarna av studien flaggade en bias >0,5 % (5 mmol/mol) inom 95 % CI. Precisionen utvärderades vid 3HbA1c koncentrationer 30, 48, och 75 mmol/mol (4,9 %, 6,5 % och 9,0 %), CV’s >2,0 % (>3,0 %) flaggades av studiens författare.
Utvärdering av kvalitet bortom certifiering
Även om många av de PNA-instrument som ingår i denna utvärdering är NGSP- och IFCC-certifierade, presterade majoriteten dåligt. Vilket indikerar att en enda årlig certifiering kanske inte är en tillräcklig indikator på kvaliteten.
Denna oberoende utvärdering belyser prestandavariabiliteten i NGSP- och
IFCC-certifierade PNA HbA1c-instrument. Även om certifiering är viktig är det
inte en garanti för en konsekvent analytisk kvalitet.
Analysinstrumentet Afinion 2 utmärkte sig som det enda instrument som uppfyllde alla prestandakriterier inklusive den strängare >4σ, tröskevärde enligt IFCC’s riktlinjer för kliniska studier. Dessa resultat understryker vikten av individuell validering av analysinstrument och stöder användningen av Afinion 2 både i rutinmässiga och i mer avancerade kliniska miljöer.
För att ta del av hela studien, metodiken och den statistiska analysen bakom dessa resultat rekommenderar vi att du läser den fullständiga publicerade utvärderingen av Lenters-Westra et al.
Referenser
- Lenters-Westra E, Singh P, Vetter B, English E. Challenges in Hb A1c Point-of-Care Testing: Only 5 of 19 Hb A1c Point-of-Care Devices Meet IFCC and NGSP Certification Criteria on Independent Evaluation. Clin Chem. Published online May 26, 2025. doi:10.1093/clinchem/hvaf059
- Lenters-Westra E, Slingerland RJ. Three of 7 hemoglobin A1c point-of-care instruments do not meet generally accepted analytical performance criteria. Clin Chem. 2014;60(8):1062–1072. doi:10.1373/clinchem.2014.224311
- Lenters-Westra E, English E. Evaluation of four HbA1c point-of-care devices using international quality targets: are they fit for the purpose? J Diabetes Sci Technol. 2018;12(4):762–770. doi:10.1177/1932296818785612
- National Glycohemoglobin Standardization Program (NGSP). College of American Pathologists (CAP) Survey Data. Available from: https://ngsp.org/CAPdata.asp.
- National Glycohemoglobin Standardization Program (NGSP). HbA1c assay interferences. Available from: https://ngsp.org/interf.asp.
- Kushner PR, Fonseca V, Nichols JH, Shubrook JH, Miller E, Wright E, DeFilippi C, Vassalotti JA. Clinical need for point-of-care testing for diabetes in Clinical and Laboratory Improvement Amendments–waived settings. Clin Diabetes. 2024; doi:10.2337/cd24-0071.



